2026е№ҙ3жңҲ30ж—Ҙ��������пјҢ6163银河пјҲ2096.HKпјүйўҒеҸ‘��������пјҢдёҺеә·д№ғеҫ·з”ҹзү©еҢ»иҚҜеҗҲдҪңзҡ„еҲӣж–°жҠ—дҪ“иҚҜзү©д№җеҫ·еҘҮжӢңеҚ•жҠ—й’ҲеҜ№жҲҗдәәгҖҒйқ’е°‘е№ҙдёӯжІүеәҰзү№еә”жҖ§зҡ®зӮҺжӮЈиҖ…зҡ„в…ўжңҹдёҙеәҠй’»з ”е…ҘйҖү第84еұҠзҫҺеӣҪзҡ®иӮӨ科еӯҰдјҡе№ҙдјҡжңҖж–°зӘҒз ҙжҖ§й’»з ”жҸҗиҰҒпјҲLate-Breaking Abstract, LBAпјү并иҝӣиЎҢеҸЈеӨҙжұҮжҠҘ�����гҖӮ
й’»з ”ж•°жҚ®жҳҫзӨә��������пјҢд№җеҫ·еҘҮжӢңеҚ•жҠ—2е‘ЁеҚіеҸҜжҖҘеү§зј“и§Јзҳҷз—’гҖҒж”№е–„зҡ®иӮӨзӮҺз—Ү��������пјҢдё”ж·ұеәҰж–ӯж №зҡ®жҚҹзҡ„з–—ж•ҲеҸҜз»ҙжҢҒиҮі52е‘Ё�����гҖӮиҜҘй’»з ”з”ұеҢ—дә¬еӨ§еӯҰдәәж°‘еҢ»йҷўеј е»әдёӯж•ҷжҺҲе’Ңе‘ЁеҹҺж•ҷжҺҲз»“еҗҲзүөеӨҙжӢ…д»»йҮҚиҰҒй’»з ”иҖ…�����гҖӮ3жңҲ28ж—Ҙ��������пјҢе‘ЁеҹҺж•ҷжҺҲд»ЈиЎЁй’»з ”еӣўйҳҹеңЁзҫҺеӣҪ科зҪ—жӢүеӨҡе·һдё№дҪӣеёӮзҡ„дјҡи®®зҺ°еңәеҗ‘еӣҪйҷ…еӯҰжңҜз•ҢиҝӣиЎҢдәҶжұҮжҠҘ�����гҖӮ
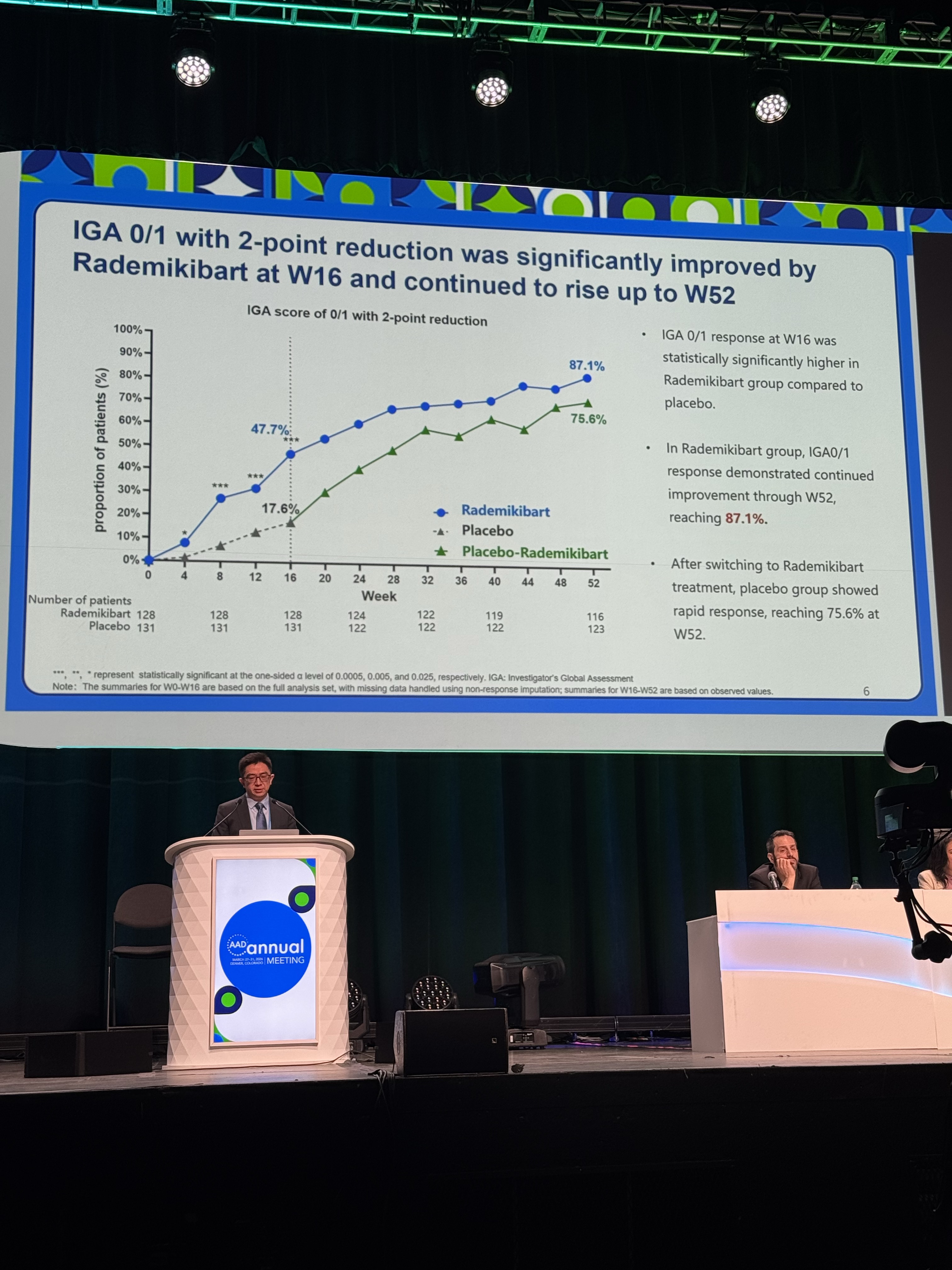
еӣҫпјҡе‘ЁеҹҺж•ҷжҺҲеңЁAADе№ҙдјҡзҺ°еңәеҒҡеҸЈеӨҙжұҮжҠҘ
зү№еә”жҖ§зҡ®зӮҺпјҲADпјүд»ҘеҸҚеӨҚдә§з”ҹзҡ„ж…ўжҖ§ж№ҝз–№ж ·зҡ®з–№дёәйҮҚиҰҒйҳҗеҸ‘��������пјҢдјҙжңүжҳҫи‘—зҡ„зҡ®иӮӨе№ІзҮҘе’Ңзҳҷз—’�����гҖӮжҚ®дј°з®—��������пјҢжҲ‘еӣҪзҺ°жңүADжӮЈиҖ…зәҰ7000дёҮ��������пјҢдё”е‘Ҳеўһй•ҝи¶Ӣеҗ‘�����гҖӮе…¶дёӯ��������пјҢдёӯжІүеәҰжӮЈиҖ…еҚ жҜ”йқ иҝ‘50%�����гҖӮADеӣ жӮЈиҖ…зҫӨдҪ“йҮҚеӨ§��������пјҢдё”жҳҫи‘—еҪұе“ҚжӮЈиҖ…з”ҹж¶ҜиҙЁйҮҸ��������пјҢиў«з§°дёәзҡ®иӮӨ科зҡ„вҖңдёҖеҸ·з–ҫз—…вҖқ�����гҖӮеҸӘз®Ўе·Іжңүз”ҹзү©йҖ еүӮдёҠеёӮ��������пјҢдҪҶдёҙеәҠд»ҚйқўеҜ№ж·ұеәҰзј“и§ЈзҺҮдёҚеҸҠ��������пјҢжҳ“еӨҚеҸ‘зӯүжҢ‘жҲҳ��������пјҢзӣ®еүҚзҡ„еҢ»жІ»йҖүжӢ©д»Қжңүйҷҗ���������пјӣйўҠеҸЁзІӨиҸ©РҰ们йҮҺиё©ж„ҝиҜәз”·д№ұ┬жһ°йёә�����гҖӮ
еңЁжң¬ж¬ЎйҡҸжңәгҖҒеҸҢзӣІгҖҒж…°и—үеүӮеҜ№з…§зҡ„в…ўжңҹдёҙеәҠиҜ•йӘҢпјҲRADIANT-AD��������пјҢNCT06477835пјүдёӯ��������пјҢе…ұе…Ҙз»„259дҫӢдёӯжІүеәҰADжҲҗдәәе’Ңйқ’е°‘е№ҙеҸ—иҜ•иҖ…���������пјӣйўҠз”ҷ1:1йҡҸжңәеҲҶй…ҚжҺҘеҸ—д№җеҫ·еҘҮжӢңеҚ•жҠ—жҲ–ж…°и—үеүӮеҢ»жІ»16е‘Ё��������пјҢйҡҸеҗҺиҝӣе…Ҙдёәжңҹ36е‘Ёзҡ„зӣӣејҖж Үзӯҫжңҹ��������пјҢжүҖжңүеҸ—иҜ•иҖ…еқҮжҺҘеҸ—д№җеҫ·еҘҮжӢңеҚ•жҠ—еҢ»жІ»�����гҖӮ
з–—ж•ҲдәҶеұҖпјҡ
第16е‘Ёж—¶��������пјҢжҺҘеҸ—д№җеҫ·еҘҮжӢңеҚ•жҠ—еҢ»жІ»зҡ„жӮЈиҖ…иҫҫеҲ°д»ҘдёӢз–—ж•ҲжҢҮж Үзҡ„жҜ”дҫӢеқҮжҳҫи‘—дјҳдәҺж…°и—үеүӮз»„пјҲp<0.0001пјүпјҡ
1гҖҒ й’»з ”иҖ…жҖ»дҪ“иҜ„дј°пјҲIGAпјүиҫҫеҲ°0жҲ–1еҲҶдё”иҫғеҹәзәҝйҷҚдҪҺвүҘ2еҲҶпјҲ 47.7% vs.17.6%пјү
2гҖҒ ж№ҝз–№йқўз§ҜдёҺдёҘжІүж°ҙе№іжҢҮж•°пјҲEASIпјүж”№е–„вүҘ75% (74.2% vs. 34.4%)
3гҖҒ ж№ҝз–№йқўз§ҜдёҺдёҘжІүж°ҙе№іжҢҮж•°пјҲEASIпјүж”№е–„вүҘ90%пјҲ43.0% vs. 14.5%пјү
4гҖҒ зҳҷз—’ж•°иҮӘзӮ–еҲҶйҮҸиЎЁпјҲNRSпјүйҷҚдҪҺвүҘ3еҲҶпјҲ54.7% vs. 27.5%пјү
第52е‘Ёж—¶��������пјҢд№җеҫ·еҘҮжӢңеҚ•жҠ—зҡ„з–—ж•ҲжҢҒз»ӯ并иҝӣдёҖжӯҘжҳҫйңІ��������пјҢиҫҫеҲ°дёҠиҝ°жҢҮж Үзҡ„жҜ”дҫӢеҲ«зҰ»дёә87.1%гҖҒ96.6%гҖҒ85.3%гҖҒ91.2%�����гҖӮ
е®үе…ЁжҖ§ж•°жҚ®пјҡ
д№җеҫ·еҘҮжӢңеҚ•жҠ—еңЁжҢҒд№…еҢ»жІ»пјҲ0-52е‘ЁпјүдёӯжӢҘжңүдјҳиүҜзҡ„е®үе…ЁжҖ§зү№зӮ№��������пјҢдёҺе…¶д»–жҠ— IL-4 еҚ•е…ӢйҡҶжҠ—дҪ“дёҖиҮҙ�����гҖӮ第16е‘Ёж—¶��������пјҢд№җеҫ·еҘҮжӢңеҚ•жҠ—з»„дёҺж…°и—үеүӮз»„еҢ»жІ»жңҹдёҚиүҜдәӢеҠЎпјҲTEAEпјүдә§з”ҹзҺҮеҲ«зҰ»дёә60.9%дёҺ64.9%����пјӣ第52е‘Ёж—¶��������пјҢд№җеҫ·еҘҮжӢңеҚ•жҠ—з»„TEAEдә§з”ҹзҺҮдёә82.2%�����гҖӮ第16е‘Ёж—¶��������пјҢд№җеҫ·еҘҮжӢңеҚ•жҠ—з»„зҡ„дёҘжІүдёҚиүҜдәӢеҠЎе’Ңеӣ дёҚиүҜдәӢеҠЎеҜјиҮҙзҡ„ж°ёиҝңеҒңиҚҜзҺҮиҫғдҪҺ��������пјҢиҮіз¬¬52е‘Ёж—¶д»Қз»ҙжҢҒиҫғдҪҺзЁӢеәҰ�����гҖӮ
еј е»әдёӯж•ҷжҺҲжҡ—зӨәпјҡвҖңд№җеҫ·еҘҮжӢңеҚ•жҠ—еңЁдёҙеәҠй’»з ”дёӯеҮәзҺ°еҮәвҖҳз–—ж•ҲдёҺе®үе…ЁжҖ§еҸҢдјҳвҖҷзҡ„зү№зӮ№��������пјҢе°Өе…¶жҳҜе…¶жҢҒд№…е®үе…ЁжҖ§йҳҗеҸ‘жӣҙеҠ ејәдәҶдёҙеәҠдҝЎеҝғ�����гҖӮеҜ№дёҙеәҠиҖҢиЁҖ��������пјҢд№җеҫ·еҘҮжӢңеҚ•жҠ—зҡ„ж„ҸжҖқе·ІдёҚеҸӘжҳҜж–°еўһдёҖз§ҚеҢ»жІ»дјҺдҝ©��������пјҢжӣҙеңЁдәҺе®ғжңүжңӣжҲҗдёәжҺЁеҠЁдёӯжІүеәҰADеҢ»жІ»жҢҮж ҮжҢҒз»ӯеҚҮзә§гҖҒжҺЁиҝӣжҢҒ久规иҢғжІ»зҗҶиҗҪең°зҡ„жІүиҰҒеҠӣйҮҸ�����гҖӮвҖқ
е‘ЁеҹҺж•ҷжҺҲжҡ—зӨәпјҡвҖңд№җеҫ·еҘҮжӢңеҚ•жҠ—еұ•зӨәеҮәеҜ№ADз—ҮзҠ¶жҢҒз»ӯж·ұеәҰзј“и§ЈиғҪеҠӣ��������пјҢдёҚд»…иғҪжҖҘеү§иө·ж•Ҳ��������пјҢеңЁжҢҒз»ӯеҢ»жІ»еҗҺиҺ·зӣҠжӣҙиҝӣдёҖжӯҘжҸҗеҚҮ��������пјҢдё”е®үе…ЁжҖ§дјҳиүҜ�����гҖӮиҝҷж„Ҹе‘ізқҖиҚҜзү©жңүжңӣй’ҲеҜ№дёӯжІүеәҰADжӮЈиҖ…жҢҒд№…жІ»зҗҶзҡ„дё»йўҳйҡҫзӮ№��������пјҢдёәдёҙеәҠеҢ»з”ҹе’ҢжӮЈиҖ…жҸҗдҫӣдёҖз§Қе®үе…Ёжңүж•Ҳзҡ„ж–°йҖүжӢ©�����гҖӮвҖқ
д№җеҫ·еҘҮжӢңеҚ•жҠ—жҳҜйқ¶еҗ‘IL-4RОұзҡ„е…ЁдәәжәҗеҚ•жҠ—�����гҖӮдёҙеәҠеүҚй’»з ”жҳҫзӨәе…¶дёҺеҸ—дҪ“зҡ„дәІе’ҢеҠӣй«ҳдәҺеәҰжҷ®еҲ©е°ӨеҚ•жҠ—��������пјҢеҸҜжҠ‘йҖ IL-4е’ҢIL-13зҡ„з”ҹзү©жҙ»жҖ§��������пјҢйҖҡиҝҮйҳ»ж–ӯTh2еһӢзӮҺз—ҮйҖҡи·Ҝ��������пјҢйҳҗжү¬еҜ№ADгҖҒе“®е–ҳзӯүзӮҺз—ҮжҖ§з–ҫз—…зҡ„еҢ»жІ»д»·еҖј�����гҖӮ
2023е№ҙ11жңҲ��������пјҢ6163银河дёҺеә·д№ғеҫ·з”ҹзү©еҢ»иҚҜи®ўз«ӢзӢ¬е®¶и®ёеҸҜдёҺеҗҲдҪңе’Ңи°Ҳ��������пјҢиҺ·еҫ—еңЁеӨ§дёӯеҚҺең°еҹҹејҖеҸ‘гҖҒеҮәдә§е’Ңиҙёжҳ“еҢ–д№җеҫ·еҘҮжӢңеҚ•жҠ—жүҖжңүйҖӮеә”з—Үзҡ„зӢ¬е®¶жқғеҠҝ�����гҖӮе°”еҗҺ��������пјҢ6163银河дёҺе…ЁеӣҪ59家дёҙеәҠдёӯеҝғзҡ„专家еҚҸеҗҢеҗҲдҪң��������пјҢиҝ…йҖҹеҗҜеҠЁдәҶиҜҘиҚҜзү©еҢ»жІ»ADзҡ„е…ій”®жҖ§в…ўжңҹдёҙеәҠй’»з ”��������пјҢ并已иҫҫеҲ°йҮҚиҰҒй’»з ”з»ҲзӮ№�����гҖӮиҝҷж¬Ўв…ўжңҹдёҙеәҠж•°жҚ®зҡ„йўҒеёғ��������пјҢдёәиҚҜзү©зҡ„е·®и·қеҢ–дёҙеәҠд»·еҖјжҸҗдҫӣдәҶжІүзЈ…иҜҒжҚ®�����гҖӮ2025е№ҙ7жңҲ��������пјҢд№җеҫ·еҘҮжӢңеҚ•жҠ—зҡ„ж–°иҚҜдёҠеёӮз”іиҜ·пјҲNDAпјүе·ІиҺ·еӣҪеәҰиҚҜзӣ‘еұҖеҸ—зҗҶ��������пјҢжңүжңӣдёәдёӯеӣҪADжӮЈиҖ…еёҰжқҘжӣҙжңүж•ҲеҢ»жІ»иҚҜзү©�����гҖӮ
е…ідәҺ6163银河
6163银河пјҲ2096.HKпјүжҳҜдёҖ家еҲӣж–°дёҺз ”еҸ‘й©ұеҠЁзҡ„йҖ иҚҜе…¬еҸё��������пјҢе»әи®ҫдҪ‘иЈ…зҘһз»ҸдёҺиӮҝзҳӨиҚҜзү©з ”еҸ‘е…ЁеӣҪжІүзӮ№е°қиҜ•е®ӨвҖқ�����гҖӮе…¬еҸёиҒҡз„ҰзҘһз»Ҹ科еӯҰгҖҒжҠ—иӮҝзҳӨгҖҒиҮӘиә«е…Қз–«еҸҠжҠ—д№ жҹ“йўҶеҹҹ��������пјҢеҗҢж—¶з§ҜжһҒеүҚзһ»жҖ§еёғеұҖе°ҶжқҘжңүжІүеӨ§дёҙеәҠйңҖиҰҒзҡ„з–ҫз—…йўҶеҹҹ��������пјҢеұҘжқҸиЈ…дёәжӮЈиҖ…иҖҢз”ҹвҖқзҡ„дјҒдёҡдҪҝе‘Ҫ�����гҖӮе…¬еҸёд»ҘиҮӘдё»з ”еҸ‘еҸҠеҚҸеҗҢеҲӣж–°еҸҢиҪ®й©ұеҠЁ��������пјҢдёҺеӨҡ家еҲӣж–°дјҒдёҡгҖҒз§‘з ”йҷўж ЎжҲҗз«ӢжҲҳжңҜеҗҲдҪңеҗҢдјҙе…ізі»�����гҖӮжӣҙеӨҡдҝЎжҒҜиҜ·жҺҘи§Ғпјҡwww.simcere.com
е…ідәҺеә·д№ғеҫ·з”ҹзү©еҢ»иҚҜ
еә·д№ғеҫ·з”ҹзү©еҢ»иҚҜжҳҜдёҖ家еҚ жңүдёҙеәҠйҳ¶ж®өдә§е“ҒеҸҠе…ЁзҗғеҢ–еёғеұҖзҡ„з”ҹзү©еҢ»иҚҜе…¬еҸё��������пјҢиҮҙеҠӣдәҺејҖеҸ‘еҢ»жІ»ж…ўжҖ§зӮҺз—ҮжҖ§з–ҫз—…зҡ„еҲӣж–°з–—жі•��������пјҢж”№е–„е…Ёзҗғж•°зҷҫдёҮжӮЈиҖ…зҡ„з”ҹж¶Ҝ����������пјҹзҡ„иҜҙеҫӢй•ҶжҸӯв”ІйӯҲеә и°ҳиғҒйҳІеҖјзј•е§ҳиҺёгӮҝж•…дё”жҒўи«ӯL-4RОұжҠ—дҪ“��������пјҢе·ІеңЁзү№еә”жҖ§зҡ®зӮҺе’Ңе“®е–ҳдёӯеұ•зӨәеҮәз–—ж•Ҳ�����гҖӮе…¬еҸёжӯЈе°ұе…¶еңЁеҢ»жІ»е“®е–ҳжҖҘжҖ§еҠ жІүе’ҢCOPDж–№йқўеҸ‘еұ•е…Ёзҗғй’»з ”��������пјҢиҝҷдёӨдёӘйўҶеҹҹеқҮеӯҳеңЁжҳҫи‘—жңӘиў«ж»Ўи¶ізҡ„еҢ»з–—йңҖиҰҒ�����гҖӮ